碱金属概述
预计阅读时间: 7 分钟
碱金属的性质
碱金属性质概述
-
碱金属大多为银白色固体(铯 Cs 略带金色)、密度小柔软、熔沸点低。
-
按照从上到下,Li,Na,K,Rb,Cs,熔沸点降低、密度增大(钾反常小),与氧气反应更加复杂。
Li+OX2LiOX2
Na+OX2NaX2O,NaX2OX2
K+OX2KX2O,KX2OX2,KOX2,KOX3
-
对应的碱,除了氢氧化锂外均为强碱,且碱性依次增强。
钠单质的物理性质
- 质软。
- 银白色金属光泽。
- 常温下是固态。
- 密度比水小,比煤油大。
- 熔点低。
钠单质的化学性质
钠与氧气的反应
钠与水的反应
Na+2HX2O2NaOH+HX2↑
钠与酸的反应
与非氧化性酸(e.g. HCl)发生反应:
- 2Na+2HCl2NaCl+HX2↑。
- 2Na+HX2O2NaOH+HX2↑。
其中与强酸的反应一般比与水的更剧烈。
钠与盐的反应
与盐溶液反应:
-
先和水生成碱。
-
后发生碱和盐的反应。
2Na+2HX2O+CuSOX4HX2↑+NaX2SOX4+Cu(OH)X2↓
-
现象:同时有气体和沉淀产生。
与熔融盐盐发生置换反应:
2Na+CuSOX4Cu+NaX2SOX4
钠的应用
- 高压钠灯。
- 钠钾合金用作原子反应堆的导热剂。
钠冶炼金属:
-
通常用于冶炼制取纯度高的金属,尤其是熔融态还原金属氯化物。
-
钠还原四氯化钛(TiCl₄)是工业制钛的重要方法(亨特法):
此反应在惰性气氛中进行,生成的海绵钛经熔炼后用于航空、医疗等领域。
亨特法逐渐被用镁还原的克劳尔法所替代。
-
此外,还可以用于冶炼锆(Zr)、铌(Nb)、钽(Ta)。
钠的氧化物
氧化钠的性质
作为碱性氧化物,与酸、水、酸性氧化物的反应:
NaX2O+2HClNaX2O+HX2ONaX2O+COX22NaCl+HX2O2NaOHNaX2COX3
同时存在 2NaX2O+OX22NaX2OX2 在加热条件下生成。
过氧化钠的性质
类似氧化钠的:
2NaX2OX2+4HCl2NaX2OX2+2HX2O2NaX2OX2+2COX24NaCl+2HX2O+OX24NaOH+OX22NaX2COX3+OX2
可以进行氧气供给。
NaX2OX2+SOX2NaX2OX2+SOX3NaSOX4NaSOX4+OX2
这是因为其具有强氧化性,另外其还具有漂白性,可以用于杀菌消毒。
钠的氧化物题型
关于 NaX2OX2 的增重:
- NaX2OX2 与 HX2O 反应,相当于增加了 HX2 的重量。
- NaX2OX2 与 COX2 反应,相当于增加了 CO 的重量。
因此:ag 的 HX2,CO 混合气体与足量氧气点燃,生成的气体通过足量过氧化钠,增重 ag。
钠单质长期暴露在空气中,会变为 NaX2COX3 固体。
钠的碳酸(氢)盐
套管实验
理论:NaX2COX3 比 NaHCOX3 更碱、更溶、更稳定。
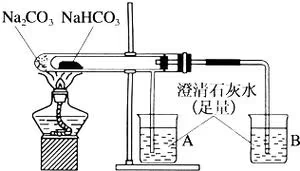
- 外层:NaX2COX3,无明显现象。
- 内层:NaHCOX3,塞蘸有无水硫酸铜的棉花,插入澄清石灰水中。
类似的结论有 OHX−+HCOX3X+HX2O+COX3X2−。
半径法
- 向 NaOH 溶液中通入二氧化碳。
- 向得到的溶液中加入稀盐酸,记录二氧化碳产生量与加入盐酸的量的折线图。
从折点开始画圆,半径为左右较小的长度,圆内平阶段发生碳酸钠的反应,前发生氢氧化钠的反应。
海水制碱
氨碱法(索尔维制碱法):
经典问题:
工业流程:
-
循环使用 NaHCOX3 分解产生的氨气。
-
使用碳酸钙制取 Ca(OH)X2 与 NHX4Cl 反应,循环利用氨气。
-
缺点:产生 CaClX2 无用物质,NaCl 利用率低。
联合制减法(侯氏制碱法):
